|
|
E' una specie chimica capace di cedere un protone ad un'altra specie
chimica.
|
|
|
Acido che contiene due protoni trasferibile per molecola (es.H2SO4,
H2S).
|
|
|
Acido con più di un protone trasferibile per molecola.
|
|
|
La sostanza che acquista elettroni durante una reazione di ossido- riduzione. Nel corso della reazione l'agente ossidante si riduce; un forte agente ossidante, reagendo, diventa un debole agente riducente.
|
|
|
La sostanza che durante una reazione di ossido-riduzione forma con facilità ioni positivi; come è prevedibile in base alla bassa elettronegatività, i più attivi sono i metalli alcalini, seguiti da quelli alcalino-terrosi. Fra tutti gli elementi il cesio è il più forte agente riducente.
|
|
|
Polo negativo. Elettrodo su cui avviene la semireazione di ossidazione.
|
|
|
Specie chimica capace di accettare un protone da un'altra specie
chimica.
|
|
|
Consiste, scritti i reagenti ed i prodotti della reazione, nel fare in
modo che il numero ed il tipo degli atomi presenti nei reagenti sia
esattamente uguale al numero ed al tipo di atomi presenti nei prodotti.
Bilanciare un'equazione di reazione significa determinare i coefficienti
di reazione.
|
|
|
Branca che si occupa dei composti e delle reazioni chimiche
riguardanti i processi che avvengono nei sistemi viventi.
|
|
|
La variazione di entalpia dovuta alla reazione che dà origine ad una
mole di composto a partire dagli elementi che lo costituiscono.
|
|
|
Calore svolto o assorbito nel corso di una reazione
chimica.
|
|
|
Spazio che intercorre tra due urti successivi di una stessa
particella.
|
|
|
Polo positivo. Elettrodo su cui avviene la semireazione di riduzione.
|
|
|
Sistema capace di produrre energia elettrica. E' caratterizzata dalle
due coppie REDOX che danno origine alle
reazione anodica ed alla reazione catodica.
|
|
|
Metodo per separare un sistema
eterogeneo nelle fasi che lo costituiscono,
fondato sulla differenza di densità sfruttando l'azione della forza
centrifuga.
|
|
|
La chimica è la scienza della natura che studia la composizione, la
struttura e le proprietà delle sostanze, ed anche le trasformazioni che
queste sostanze subiscono.
|
|
|
Si interessa della identificazione delle sostanze chimiche, della
determinazione della quantità delle varie specie presenti in un miscuglio
e della separazione dei miscugli nei loro singoli componenti.
|
|
|
Studia la struttura della materia e le variazioni energetiche che si
verificano nel corso delle trasformazioni chimiche e fisiche. Questo
settore fornisce le basi teoriche per trattare i fenomeni osservati negli
altri campi della chimica.
|
|
|
La chimica inorganica è la branca della chimica che tratta delle
proprietà e del comportamento di tutti gli elementi e dei loro composti
con l'eccezione dei composti del carbonio (tranne pochi). La maggior parte
dei composti del carbonio sono oggetto di studio della chimica organica.
|
|
|
In origine si limitava a studiare i composti che si ottengono dagli
organismi viventi, ma attualmente sono oggetto di studio anche gli
idrocarburi (composti di carbonio e idrogeno) e i loro derivati.
|
|
|
Studio delle velocità di reazione e la loro dipendenza dalle
condizioni sperimentali.
|
|
|
Fattore che consente di valutare lo scostamento del comportamento
ideale in funzione della pressione e della temperatura.
|
|
|
Intensità della corrente che circola nella soluzione tra due
elettrodi di sezione unitaria posti a distanza unitaria sotto la
differenza di potenziale di 1 Volt.
|
|
|
Coppia formata dalla forma ossidata e ridotta di una specie
chimica.
|
|
|
Costante caratteristica di ciascuna reazione, per una
certa temperatura. In generale, se reagiscono a molecole di A con b
molecole di B ecc. per formare m molecole di M, n di N, ecc., secondo la
reazione di equilibrio aA+bB+...=mM+nN+... l'espressione della costante
è:
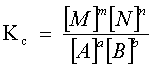
|
|
|
Strumento che permette
al chimico di determinare la disposizione spaziale degli atomi, degli ioni
o delle molecole che costituiscono i cristalli attraverso lo scattering
(la diffusione) dei raggi x.
|
|
|
Temperatura alla quale la tensione di vapore del liquido uguaglia la
pressione esterna.
|
|
|
Passaggio di un gas attraverso un piccolo foro di una parete sottile.
|
|
|
Velocità con un cui un gas effonde. E' proporzionale al numero di
urti al secondo e quindi alla velocità quadratica media.
|
|
|
E' un composto chimico di atomi di un solo tipo. Il ferro, ad esempio,
è composto interamente di atomi di ferro, che sono differenti dagli atomi
di ossigeno
|
|
|
In una cella galvanica, elettrodo che
funge da semplice conduttore e non partecipa direttamente alla
semireazione (ad es., elettrodo ad idrogeno H+/H2).
|
|
|
E' una grandezza in relazione con l'attrazione che un atomo esercita
sugli elettroni quando è in combinazione con altri elementi: è la
capacità che ha un atomo in una molecola di attrarre gli elettroni verso
di sé.
|
|
|
Elettroni responsabili dell'attività chimica di ciascun elemento
cioè dell'interazione con altri atomi.
|
|
|
Energia necessaria ad allontanare completamente un elettrone da un
atomo isolato.
|
|
|
|
|
|
Qualunque parte di un sistema omogeneo e fisicamente distinta dalle
altre parti.
|
|
|
Metodo per separare un sistema
eterogeneo nelle fasi che lo costituiscono, basato
sulla differenza di dimensioni delle particelle che costituiscono le fasi:
il sistema passa attraverso un materiale poroso che funziona da filtro..
|
|
|
E' l'elemento più elettronegativo e l'agente ossidante più attivo tra gli elementi chimici. Esso reagisce formando lo ione fluoruro, che è il più debole agente
riducente.
|
|
|
Differenza di potenziale che si viene a creare fra due elettrodi di
una cella galvanica e che genera un flusso
di elettroni dall'anodo al catodo.
Dipende anche dalla temperatura e dalle concentrazioni delle specie in
soluzione.
|
|
|
Elementi costituiti da atomi senza elettroni
di valenza e che quindi non hanno alcuna attività chimica.
|
|
|
|
|
|
Relazione matematica che permette di valutare il peso molecolare
incognito di un gas rapportando la sua velocità
di effusione a quella di un gas di peso molecolare noto.
|
|
|
A temperatura costante, la concentrazione di un gas debolmente
solubile in un liquido (cioè la massa o il numero di moli di un gas che
si scioglie in un dato volume di un liquido) è direttamente proporzionale
alla pressione parziale del gas.
|
|
|
La variazione di entalpia connessa ad una trasformazione chimica o
fisica è pari alla somma delle variazioni di entalpia dei singoli stadi
attraverso i quali avviene o si immagina possa avvenire la reazione
stessa.
|
|
|
Legge strettamente valida per soluzioni
ideali (o quasi ideali) che
mette in relazione, a temperatura costante, il valore della pressione di
vapore di una soluzione con la composizione di questa e con i valori della
pressione di vapore delle singole specie che la costituiscono. Per una
soluzione costituita da due componenti, la legge è espressa dalla
relazione:
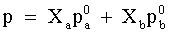 . .
La composizione della fase vapore in equilibrio con una
soluzione è diversa da quella della soluzione stessa (salvo il caso
particolare di soluzioni in cui:
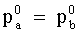
|
|
|
Numero di moli (ni) di un soluto (i) contenuti in 1000 g di
solvente.
|
|
|
Rapporto fra il numero di moli (ni) del componente (i) ed
il numero di moli totali presenti in soluzione.
|
|
|
Numero di moli (ni) di un soluto (i) contenuti in un litro
di soluzione. Poiché il volume varia con la
temperatura, a temperature diverse corrispondono valori diversi di M.
|
|
|
Relazione che mostra come il potenziale di elettrodo di una generica coppia
redox sia in funzione delle concentrazioni della forma ossidata e
della forma ridotta ciascuna elevata ad un esponente pari al coefficiente
di reazione.
|
|
|
I tre numeri che caratterizzano ogni orbitale.
|
|
|
Somma dei protoni e dei neutroni nel nucleo.
|
|
|
Definisce il senso del moto dell'elettrone intorno al proprio asse.
|
|
|
Indica l'orientamento dell'orbitale rispetto a
tre assi cartesiani arbitrariamente scelti.
|
|
|
Indica il livello energetico cui appartiene l'orbitale.
Può assumere solo valori interi positivi (1, 2, 3, ...) e dà un'idea
approssimata della distanza dell'elettrone dal nucleo.
|
|
|
Specifica la forma spaziale dell'orbitale.
Può assumere valori interi compresi tra 0 ed (n-1) dove. n=numero
quantico principale.
|
|
|
Superficie chiusa che racchiude il volume di spazio nel quale la
probabilità di trovare l'elettrone è circa il 90%.
|
|
|
Trasformazione chimica nella quale vengono perduti elettroni
da un atomo o da un gruppo di atomi.
|
|
|
Fenomeno per cui atomi neutri con elettroni spaiati subiscono
l'effetto di un campo magnetico.
|
|
|
Numero di grammi di un componente in 100 g di soluzione.
|
|
|
Numero di litri di un componente contenuti in 100 l di soluzione.
|
|
|
La media ponderata di tutti gli isotopi di un elemento.
|
|
|
Cella galvanica formata da due
elettrodi dello stesso metallo M immersi in due soluzioni contenenti lo
stesso ione M+n ma a due concentrazioni diverse.
|
|
|
Molecola di grandi dimensioni costituita da unità semplici che si
ripetono e sono tenute insieme da legami chimici.
|
|
|
E' una misura di quanto strettamente un atomo tiene legati i suoi
elettroni: corrisponde, infatti, alla quantità di energia necessaria per
separare un elettrone dall'atomo.
|
|
|
(Potenziale di elettrodo standard). Si calcola misurando la f.e.m.
di una cella galvanica formata dalla coppia
in esame e dalla coppia H+/H2 in condizioni
standard.
|
|
|
Secondo quanto suggerito da Wolfgang Pauli nel 1924, due elettroni
qualsiasi di un atomo non possono avere uguali tutti e quattro i numeri
quantici. Questo assunto influenza il modo in cui le proprietà
chimiche di un elemento dipendono dal suo numero atomico.
|
|
|
Temperatura alla quale il solido ed il liquido coesistono in
equilibrio col vapore.
|
|
|
Quantità di energia liberata da un elettrone passando da un livello
energetico a quello più vicino a più bassa energia.
|
|
|
Processo per cui, date alcune specie chimiche, A, B, dette reagenti,
queste interagiscono tra di loro trasformandosi in specie chimiche diverse
X, Y, dette prodotti della reazione.
|
|
|
Numeri (abitualmente si omette il numero 1) che, nelle equazioni di
reazione, compaiono davanti ai simboli delle diverse specie chimiche.
|
|
|
Variazione, nell'unità di tempo, del numero di moli di un
reagente o di un prodotto.
|
|
|
Trasformazione chimica nella quale vengono acquistati
elettroni da un atomo o da un gruppo di atomi.
|
|
|
Metodo per separare un sistema
eterogeneo nelle fasi che lo costituiscono,
fondato sulla differenza di densità sfruttando l'azione della forza di
gravità.
|
|
|
Porzione qualsiasi di materia con caratteristiche e proprietà
definite.
|
|
|
Sistema formato da più fasi.
|
|
|
Miscela di due o più sostanze diverse che costituiscono una sola fase.
|
|
|
Soluzione in cui è nulla l'entalpia di mescolamento.
|
|
|
Soluzione reale costituita da due o più sostanze le cui molecole
hanno dimensioni e struttura molto simile.
|
|
|
In un processo elettrolitico in cui riduzione ed ossidazione
comportano sviluppo di gas agli elettrodi, tensione addizionale necessaria
per fare avvenire le reazioni di ossidoriduzione agli elettrodi. Dipende
dalla natura dei gas e dalla natura dell'elettrodo.
|
|
|
Strumento di laboratorio che opera nell'ultravioletto, nel visibile e
nell'infrarosso, inviando fasci di luce di diverse lunghezze d'onda su
campioni liquidi o gassosi. In questo modo il chimico può determinare la
configurazione elettronica e la disposizione degli atomi nelle molecole.
|
|
|
(a risonanza magnetica nucleare). Strumento che sottopone il campione,
immerso in un forte campo magnetico, ad una radiofrequenza. L'assorbimento
di questa energia da parte del campione fornisce informazioni sui legami
intramolecolari.
|
|
|
In un processo elettrolitico, tensione che occorre per fare avvenire
le reazioni di ossidoriduzione agli elettrodi.
|
|
|
Modello che permette di derivare da semplici considerazioni meccaniche
una relazione tra la temperatura assoluta e l'energia cinetica media
traslazionale che formano un sistema gassoso ideale.
|